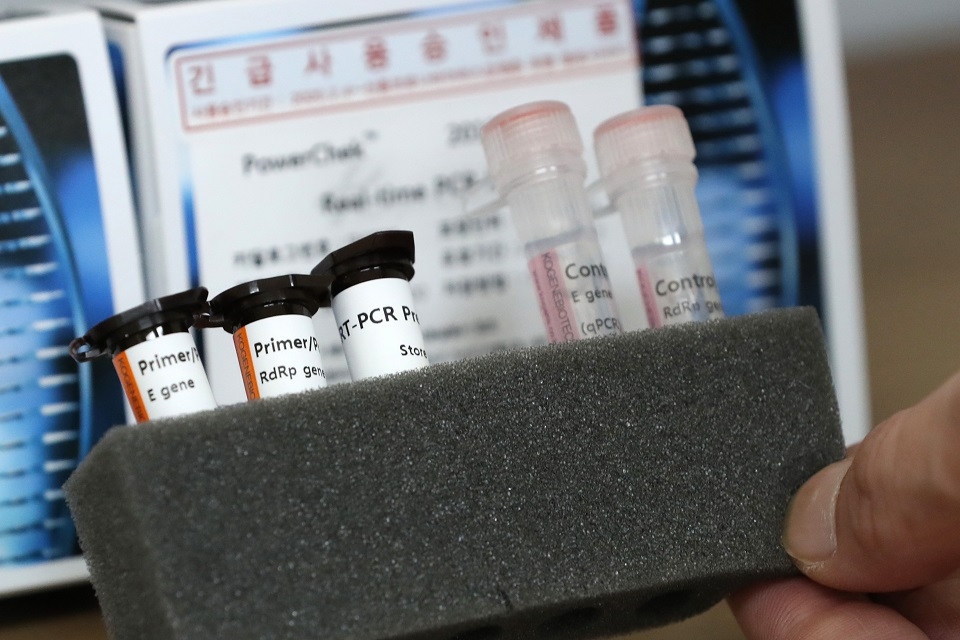
[뉴시안=박현 기자]국내에서 제조한 신종 코로나바이러스 감염증(코로나19) 진단키트가 부정확하다는 미국 하원의원의 주장에 대해 질병관리본부와 식품의약품안전처(이하 식약처)가 잇따라 반박하고 나섰다.
권준욱 질병관리본부 중앙방역대책본부 부본부장은 15일 정례 브리핑을 통해 “WHO(세계보건기구)가 권고하는 최종 확진 검사법은 바이러스 존재 자체를 확인하는 RT-PCR(실시간 역전사중합효소연쇄반응)뿐”이라며 “현재 어느 나라도 항체 검사나 항원 검사, 신속진단방법 등 다른 방식의 진단을 실행하고 있지는 않은 상황”이라고 말했다.
이어 “국내 승인 후 현재 확진 검사에 사용하고 있는 진단키트 4종류에 대해서는 미국 식품의약국(FDA)에서도 승인을 진행 중인 것으로 알고 있다”면서 “중앙방역대책본부의 입장은 국내 진단키트 사용에 대해 지속적으로 모니터링하고 있으며, 미국에서 다른 판단이 나오리라고는 생각하지 않고 있다”고 덧붙였다.
식약처도 15일 “현재 국내 긴급사용 승인된 5개 코로나19 진단시약은 모두 유전자 검출검사법(RT-PCR)을 사용하는 제품으로, 질병관리본부 등 관련 기관 검증을 완료했다”며 “해당 제품의 진단 정확도는 대한진단검사의학회를 통해 모니터링하고 있으며, 현재까지 진단오류에 대한 부작용은 보고된 바 없다”고 밝혔다.
이와 함께 “미국 하원의원이 문제 제기한 항체검사방법은 국내에서 활용되지 않고 있다”며 미국 해당 하원의원이 언급한 진단키트는 현재 국내 보건당국이 사용하는 진단키트와 무관하다는 입장을 밝혔다. 아울러 “미 FDA에서 긴급사용 승인한 4개의 코로나19 진단제품도 국내와 동일하게 유전자 검출방식을 사용한 것”이라고 덧붙였다.
앞서 국내에서 제조한 코로나19 진단키트와 관련해 미 FDA가 부적절하다는 의견을 냈다는 주장이 미국 하원의원을 통해 나온 바 있다. 미국 NBC뉴스 등에 따르면 마크 그린 공화당 의원은 지난 11일 미 하원 관리개혁위원회 청문회에서 “FDA가 서면 답변에서 ‘한국의 진단키트는 적절하지 않으며, 응급용으로도 미국에서 사용되는 데 동의하지 않는다’고 밝혔다”고 언급했다.
한편, 국내 긴급사용 승인된 코로나19 진단시약은 13일 바이오세움의 제품이 새로 승인받으면서 코젠바이오텍, 씨젠, 솔젠트, 에스디바이오센서의 제품과 함께 모두 5개로 늘었다.
